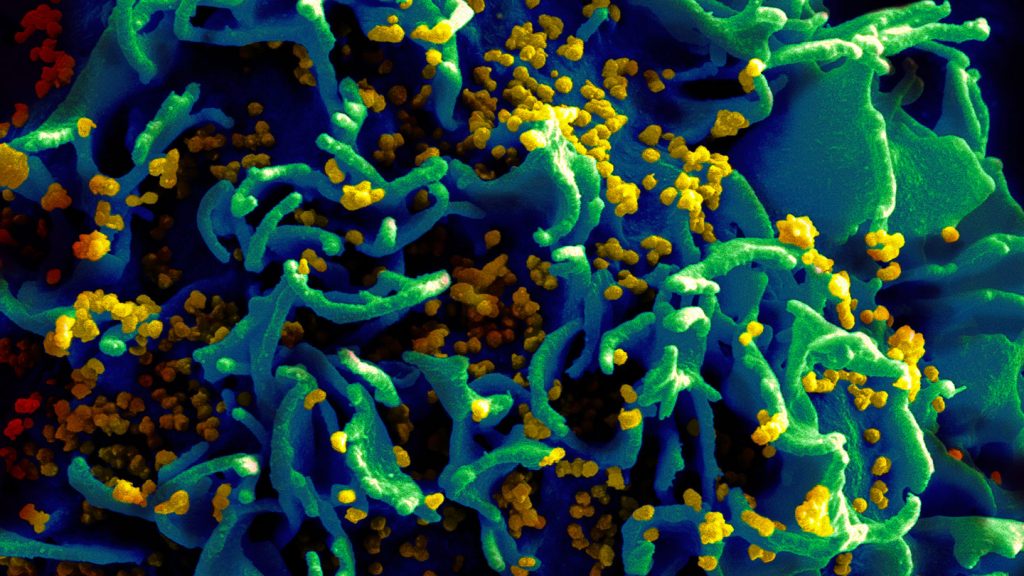
چگونه اچ آی وی موجب ایدز می شود
چگونه اچ آی وی موجب ایدز می شود : کانون توجه موسسه ملی آلرژی و بیماری های عفونی (NIAID) پژوهشی است که به بیماریزایی ویروس بیماری نقص ایمنی اکتسابی (HIV) اختصاص داده شده است مکانیسم پیچیده ای که منجر به تخریب سیستم ایمنی بدن فرد آلوده به اچ آی وی می شود. درک دقیق اچ آی وی و اینکه چگونه عفونت را بوجود آورده و باعث سندرم نقص ایمنی اکتسابی (AIDS)می شود دارای اهمیت زیادی است زیرا هدف آن شناسایی و توسعه داروهای موثر و واکسن برای مبارزه با اچ آی وی و ایدز است. این برگه آنچه که دانشمندان در مورد این فرایند در حال یادگیری هستند را خلاصه سازی کرده است و واژه نامه مختصری از اصطلاحات را فراهم می کند.
بیماری اچ آی وی به عنوان یک زوال تدریجی عملکرد سیستم ایمنی مشخص شده است. مهمترین آنها، سلول های ایمنی بسیار مهم به نامCD4 + T هستند سلول هایی که در طول دوره عفونت غیر فعال و کشته می شوند. این سلول ها، گاهی به نام “سلول های کمکیT ،” نقش اصلی را در واکنش های ایمنی بازی می کند، و سلول های پبام رسان دیگر در سیستم ایمنی بدن وظایف خاص خود را انجام می دهند.
یک فرد سالم که مبتلا نشده است معمولا ۸۰۰ تا ۱۲۰۰ سلول CD4 + T در هر میلیمتر مکعب (MM3) از خون خود دارد. در طول دوره عفونت اچ آی وی، تعداد این سلول ها در خون فرد به تدریج کاهش می یابد. هنگامی که تعداد سلول های CD4 + T یک شخص کمتر از ۲۰۰ در هر میلیمتر مکعب رسید، او به طور خاص نسبت به عفونت و سرطان فرصت طلب آسیب پذیر شده که مشخصه ایدز است و مرحله نهایی بیماری اچ آی وی می باشد. افراد مبتلا به ایدز اغلب در اثر عفونت های دستگاه گوارش، ریه ها، مغز، چشم و اندام های دیگر، و همچنین بخاطر از دست دادن وزن، اسهال، بیماری های عصبی و سرطان مانند سارکوم کاپوزی و لنفوم ضعیف و ناتوان می شوند.
بیشتر دانشمندان فکر می کنند که اچ آی وی عامل ایدز است به طور مستقیم سلول های CD4 + Tرا از بین برده و یا عملکرد طبیعی را مختل می کند، و با تحریک فرایندهای دیگر عملکرد سیستم ایمنی بدن فرد را تضعیف می کند. به عنوان مثال، شبکه ای از مولکول های پیام رسان که به طور معمول واکنش های ایمنی فرد را تنظیم می کنند، در طول بیماری HIV مختل شده و توانایی فرد را برای مبارزه با عفونت های دیگر تضعیف می کند. در دوره میانیاچ آی وی، گره های لنفاوی و ارگان های ایمنی مرتبط نیز نقش عمده ای در ایجاد ایمنی ایفا می کنند که در افراد مبتلا به ایدز نیز دیده می شود.
محدوده گستردگی و شیوع اچ آی وی
اگر چه HIV برای اولین بار در سال ۱۹۸۳ شناسایی شد، بررسی نمونه خون ها که قبلا ذخیره شده بودند نشان می دهد که این ویروس در اواخر دهه هفتاد میلادی وارد جامعه ایالات متحده شده است. در ایالات متحده، ۶۱۲۰۷۸ مورد از ایدز و ۳۷۹۲۵۸ مرگ در بین افراد مبتلا به ایدز به مراکز کنترل و پیشگیری بیماری (CDC) از تاریخ ۳۰ ژوئن ۱۹۹۷ گزارش شده است. ایدز در حال حاضر دومین عامل مرگ افراد ۲۵ تا ۴۴ ساله در این کشور است. با وجود ثابت ماندن کلی تعداد موارد جدید ایدز در این کشور، بیماری همه گیر همچنان در بخش های خاصی از جمعیت، به ویژه در میان زنان و مصرف کنندگان مواد مخدر تزریقی سرعت گرفته است.
در سراسر جهان، از دسامبر سال ۱۹۹۷، حدود ۳۰۶۰۰۰۰۰ نفر مبتلا به اچ آی وی یا ایدز تخمین زده می شود، یک رقمی که پیش بینی شده است در سال ۲۰۰۰ به ۴۰ میلیون نفر رسیده باشد. بیش از ۷۵ درصد از تمام مبتلایان بزرگسال اچ آی وی از طریق مقاربت با جنس مخالف آلوده شده اند. از سال ۱۹۹۷، مرگ های مربوط بهHIV یا ایدز در سراسر جهان با رشد تصاعدی به حدود ۱۱.۷ میلیون – ۹ میلیون بزرگسال و ۲.۷ میلیون کودک- رسید.
اچ آی وی و ویروس پسگرد
اچ آی وی متعلق به یک گروه از ویروس ها به نام ویروس پسگرد می باشد، که دارای ژن هایی متشکل از مولکول های اسید ریبونوکلئی(RNA) می باشد. ژن های انسان و بیشتر موجودات دیگر از یک مولکول مرتبط، اسید دئوکسی ریبونوکلئیک (DNA) ساخته شده اند.
مانند تمام ویروس ها، اچ آی وی می تواند تنها در داخل سلول ها تکثیر شده، و ساختار سلول برای تولید مثل را تصرف کند. با این حال، تنها اچ آی وی و دیگر ویروس های بازگرد، یک بار داخل یک سلول رفته، و از یک آنزیم به نام ترانس کریپتاز استفاده می کند تا RNA را به DNA تبدیل کند، که می تواند در ژن های سلول میزبان آمیخته شود.
ویروس های کم تحرک
اچ آی وی به یک زیر گروه از ویروس های پسگرد تعلق دارد که به عنوان ویروس آهسته گستر و یا ویروس های “کم تحرک” شناخته شده اند. این دوره از عفونت با این ویروس ها با یک فاصله طولانی بین عفونت اولیه و شروع علائم جدی مشخص شده است.
دیگر ویروس های آهسته گستر گونه غیر انسانی را آلوده می کنند. به عنوان مثال، ویروس نقص ایمنی گربه سانان(FIV) و ویروس نقص ایمنی میمون ها(SIV) که میمون ها و دیگر پستانداران غیرانسان را آلوده می کند. مانند اچ آی وی در انسان، این ویروس ها در درجه اول سلول های سیستم ایمنی حیوانات را آلوده کرده، اغلب باعث بروز علائم نقص ایمنی و علائم شبیه ایدز می شوند. این ویروس ها و میزبان های آنها برای محققان مدل های سودمند، البته ناقصی، از روند بیماری اچ آی وی در انسان را فراهم کرده اند.
ساختار ویروسی HIV-1
پوشش ویروسی
اچ آی وی دارای قطری به اندازه یک ده هزارم میلیمتر بوده و کروی شکل می باشد. پوشش بیرونی این ویروس،که به عنوان پوشش ویروسی شناخته شده است، از دو لایه مولکول چربی به نام لیپید تشکیل شده است، زمانی که ذرات ویروس از سلول جوانه می زنند از غشاء سلول انسان شکل می گیرند.
آنچه در پوشش ویروسی قرار دارد پروتئین های سلول میزبان ، و همچنین ۷۲ نسخه (به طور متوسط) از یک پروتئین پیچیده اچ آی وی که از سطح پوشش جوانه زده اند می باشند. این پروتئین، که به عنوان env شناخته شده است ، شامل یک سرپوش است که از سه یا چهار مولکول به نام گلیکوپروتئین (GP) 120، و یک ساقه متشکل از سه یا چهار مولکول gp41 تشکیل شده است که ساختار پوشش ویروسی را ثابت نگه داشته اند. بسیاری از تحقیقات جهت تولید واکسن برای HIV روی این پوشش های پروتئینی متمرکز شده است.
هسته ویروسی
در داخل پوشش یک ذره بالغ اچ آی وی یک هسته گلوله مانند و یا کاپسید ، کاسپید از ۲۰۰۰ نسخه از پروتئین ویروسی P24 ، تشکیل شده است. کاپسید تنها دو رشته از HIV RNA، را احاطه کرده است که هر کدام دارای یک نسخه از نه ژن ویروس می باشند. سه ژن از آنها ، gag، pol و env، حاوی اطلاعات مورد نیاز برای پروتئین های ساختاری ذرات ویروس جدید می باشند. برای مثال، ژن env ، یک پروتئین به نام gp160 را کدگذاری کرده که توسط یک آنزیم ویروسی شکسته شده و به شکل gp120 و gp41، و دیگر اجزای env در می آید.
سه ژن نظارتی، tat, rev,nef، و سه ژن کمکی، vif، vprو vpu، شامل اطلاعات لازم برای تولید پروتئینی هستند که توانایی اچ آی وی برای آلوده کردن یک سلول را کنترل می کند، نسخه جدیدی از ویروس و یا ایجاد کننده بیماری را تولید می کند. به عنوان مثال، پروتئین کدگذاری شده توسط nef، به نظر می رسد برای تکثیر کارآمد ویروس ضروری باشد، و پروتئین کد گذاری vpu انتشار ذرات ویروس جدید از سلول های آلوده را تحت تاثیر قرار می دهد.
در انتهای هر رشته از HIV RNA یک توالی RNA به نام تکرار ترمینال طولانی (LTR) وجود دارد. لایه ای در LTR به عنوان سوئیچی جهت کنترل تولید ویروس های جدید عمل کرده و می تواند توسط پروتئین ها از اچ آی وی ویا سلول میزبان تحریک شود.
هسته اچ آی وی همچنین شامل یک پروتئین به نام P7، پروتئین نوکلئوکپسید اچ آی وی بوده؛ و سه آنزیم که مراحل بعد چرخه زندگی ویروس را انجام می دهند: تغییر ترانس کریپتاز، اینتگراز و پروتئاز می باشند. یکی دیگر از پروتئین اچ آی وی به نام P17، یا پروتئین ماتریکس اچ آی وی، که بین هسته های ویروسی و پوشش های ویروسی نهفته است .
چرخه زندگی ویروس اچ آی وی
مراحل تکثیر ویروس
- پیوستن یا ورود
- نسخه برداری و تکثیرمعکوس و سنتز DNA
- انتقال یافتن به هسته
- ادغام
- نسخه برداری یا تکثیر ویروسی
- سنتز پروتئین ویروسی
- تجمع ویروس
- انتشار ویروس
- رشد
چرخه تکرار اچ آی وی
ورود اچ آی وی به سلول ها
عفونت معمولا زمانی شروع می شود که ذره اچ آی وی، که شامل دو نسخه از RNA HIV است، با یک سلول دارای یک مولکول سطحی به نام خوشه ۴ (CD4) مواجه می شود. سلول ها با این مولکول به عنوان سلول های CD4 مثبت (CD4 +) شناخته شده اند.
یک یا چند مولکول ویروس gp120، بطور محکم به مولکول هایCD4 در سطح سلول پیوند می خورند. غشاء ویروس و جوشش سلول، فرایندی است که احتمالا شامل پوشش اچ آی وی ویک مولکول ثانویه”کرسپتور” در سطح سلول است. در همجوشی بعدی، RNA، پروتئین ها و آنزیم ویروس در سلول منتشر می شوند.
مطالعات اخیر محققان داخلی و خارجی NIAID چند کرسپتور را برای انواع مختلف گونه های اچ آی وی شناسایی کرده اند. این کرسپتورها اهداف امیدوار کننده ای برای داروهای جدید ضد اچ آی وی هستند. در مراحل اولیه بیماری اچ آی وی، در بسیاری از افراد دارای ویروس، علاوه برCD4، یک گیرنده به نام CCR5 به سلول های مورد هدفشان وارد می شود. با پیشرفت بیماری، میزان استفاده کرسپتورها گسترش می یابد، دیگر مولکول ها، به ویژه یک مولکول به نام CXCR4را نیز شامل می شود.
اگر چه سلول های CD4 + T به نظر می رسد هدف اصلی اچ آی وی باشند،اما سایر سلول های سیستم ایمنی دارای مولکول CD4 نیز در سطوح خود آلوده می شوند. در این میان سلول ها با عمر طولانی به نام مونوسیت ها و ماکروفاژها، ظاهرا می توانند مقدار زیادی از این ویروس ها را بدون کشته شدن در خود جای دهند، در نتیجه به عنوان مخازن اچ آی وی عمل می کنند. سلولهای CD4 + T نیز به عنوان مخازن مهم اچ آی وی عمل می کنند: بخش کوچکی از این سلول ها به یک شکل ثابت و غیر فعال پناهگاه اچ آی وی می باشند. فرآیندهای طبیعی سیستم ایمنی بدن ممکن است این سلول ها را فعال کرده، و به تولید ویروسهای جدید اچ آی وی منجر شود.
گسترش سلول به سلول در اچ آی وی همچنین می تواند از طریق مرحله میانی همجوشی CD4 یک سلول آلوده با سلول های سالم رخ دهد.
نسخه برداری معکوس
در سیتوپلاسم سلول، ترانس کریپتاز معکوس اچ آی وی، RNA ویروسی را به DNA تبدیل می کند ، اسید نوکلئیک شکل می گیرد که در آن سلول ژن های خود را حمل می کند. هفت مورد از ۱۱ دارو ضد ویروسی در ایالات متحده برای درمان افراد مبتلا به عفونت اچ آی وی تایید شده اند AZT ،ddC ، ddl، d4T، 3TC، نویراپین، دلاویردین که با دخالت در این مرحله از چرخه زندگی ویروس، عمل می کنند.
ادغام
DNA متعلق به اچ آی وی تازه تشکیل شده به طرف هسته سلول حرکت می کند، هنگامی که در ژن های سلول DNA HIV که “ویروس اولیه”نامیده می شود گنجانده شدند درون DNA میزبان و با کمک ادغام اچ آی وی به هم جوش می خورند. هم جوشی هدفی مهم برای توسعه و تولید داروهای جدید است.
نسخه برداری یا تکثیر
برای اینکه یک ویروس اولیه ویروس های جدید را تولید کند، نسخه RNA باید ساخته شده که می تواند توسط اندامگان پروتئین ساز سلول میزبان خوانده شود. این نسخه ها به نام (mRNA) اسید ریبونوکلئیک پیام بر بوده ، و کار mRNA (اسید ریبونوکلئیک پیام بر)نسخه برداری است ، فرایندی که شامل آنزیم های خود سلول میزبان است. ژن های ویروسی به اتفاق اندامگان سلولی این فرایند را کنترل می کنند: برای مثال، ژن tat ، پروتئینی را کدگذاری می کند که به نسخه برداری شتاب می دهد.
سیتوکین، پروتئین های درگیر در تنظیم واکنش های ایمنی معمولی، ممکن است همچنین نسخه برداری را تنظیم کند. مولکول هایی از قبیل فاکتور بافت مردگی تومور (TNF) آلفا و اینترلوکین (IL) -6، در سطوح بالایی توسط سلولهای افراد مبتلا به HIV ترشح می شوند، که ممکن است به فعال شدن سلول های اولیه HIVکمک کنند. عفونت های دیگر، توسط ارگانیسم هایی از قبیل باکترى قارچى ، نیز ممکن است نسخه برداری را افزایش دهند.
انتقال
پس از mRNA HIV در هسته سلول پردازش شد، به سیتوپلاسم منتقل می شود. پروتئین اچ آی وی دراین فرایند حیاتی می باشد: برای مثال، یک پروتئین کد گذاری شده توسط ژن rev اجازه می دهد تا mRNA پروتئین های ساختاریاچ آی وی را کدگذاری کند تا از هسته به سیتوپلاسم منتقل شوند. بدون پروتئین rev، پروتئین های ساختاری ساخته نمی شوند.
در سیتوپلاسم، ویروس، اندامگان پروتئین ساز سلول را برمی گزیند از جمله ساختارهایی به نام ریبوزوم – تا زنجیره ای طولانی از پروتئین های ویروسی و آنزیم ها را ، با استفاده از mRNA HIV به عنوان یک الگو، ایجاد کند. این فرآیند انتقال نام دارد.
پروتئین های هسته اچ آی وی که به تازگی بوجود آمده اند ، آنزیم ها و RNA فقط در داخل غشای سلول جمع آوری می شوند، در حالی که پروتئین پوشش ویروسی وارد غشاء می شود. ذرات نابالغ ویروسی که از سلول شکل گرفته و جوانه می زنند، پوششی را بدست می آورند که شامل هم سلول و هم پروتئین اچ آی وی از غشای سلولی می باشد. در طول این بخش از چرخه زندگی ویروس، هسته این ویروس نابالغ بوده و این ویروس هنوز عفونی نیست. زنجیره های طویل پروتئین ها و آنزیم ها که هسته های ویروسی نابالغ را تشکیل می دهند حال به قطعات کوچکتری توسط یک آنزیم ویروسی به نام پروتئاز تقسیم می شوند. این مرحله منجر به ذرات ویروسی عفونی می شود.
داروهایی به نام مهار کننده های پروتئاز در این مرحله از چرخه زندگی ویروس وارد عمل می شوند. چهار دارو- ساکوییناویر ،ریتوناویر، ایندیناویر و نلفیناویر-برای ورود به بازار در ایالات متحده تایید شده اند.
انتقال اچ آی وی
در میان بزرگسالان، اچ آی وی اغلب درحین مقاربت جنسی با یک فرد آلوده منتقل می شود. در هنگام مقاربت جنسی، ویروس می تواند از طریق بافت مخاط واژن، فرج، آلت تناسلی، مقعد و یا، به ندرت از طریق دهان وارد بدن شود. احتمال انتقال توسط عواملی افزایش می یابد که ممکن است به این بافت ها آسیب بزند، به ویژه دیگر بیماری های مقاربتی که باعث زخم یا التهاب شوند.
تحقیقات نشان می دهد که سلول های سیستم ایمنی بدن به نام سلولهای دندریتیک، که در مخاط وجود دارند، ممکن است فرایند عفونت را پس از مواجهه جنسی آغاز کنند که با اتصال به ویروس و حمل آن از محل عفونت به غدد لنفاوی انجام می شود که در آن دیگر سلول های سیستم ایمنی نیز آلوده می شوند.
اچ آی وی همچنین می تواند توسط تماس با خون آلوده منتقل شود، که اغلب توسط استفاده مشترک از سوزن یا سرنگ مواد مخدر می باشد که دارای مقادیری از خون حاوی ویروس آلوده می باشد. در حال حاضر خطر ابتلا به HIV از طریق انتقال خون در ایالات متحده بسیار کم است، زیرا همه فرآورده های خونی در این کشور به طور معمول برای وجود این ویروس مورد آزمایش قرار می گیرند.
تقریبا همه کودکان آلوده به اچ آی وی ویروس را قبل یا در حین تولد از مادران خود گرفته اند. در ایالات متحده، حدود ۲۵ درصد از زنان آلوده به اچ آی وی باردار تحت درمان ضد بازگرد ویروسی قرار نگرفته اند و ویروس را به نوزادان خود منتقل کرده اند. محققان NIAID از یک رژیم خاص داروی زیدوودین (AZT) حمایت کردند که می تواند خطر انتقال اچ آی وی از مادر به کودک را دو سوم کاهش دهد. پژوهش با استفاده از ترکیبی از داروهای ضد اچ آی وی تایید شده در جریان است تا مشخص کند آیا میزان انتقال را می توان بیش از این کاهش داد.
ویروس همچنین ممکن است از یک مادر شیرده آلوده به اچ آی وی به نوزاد خود منتقل می شود.
مراحل اولیه در عفونت اچ آی وی
پس از آن که اچ آی وی وارد بدن می شود، تعداد زیادی از سلول های CD4 + را آلوده کرده و به سرعت تکرار می شود. در طول این مرحله حاد یا اولیه عفونت، خون شامل بسیاری از ذرات ویروسی است که در سراسر بدن پخش می شوند، و در ارگان های مختلف، به ویژه اندامهای لنفاوی تکثیر می شود. اندامهای لنفاوی شامل گره های لنفاوی، طحال، لوزه ها و آدنوئید می باشند.
در طول مرحله حاد عفونت، تعداد سلول های CD4 + T در جریان خون ۲۰ تا ۴۰ درصد کاهش می یابند. دانشمندان هنوز نمی دانند که آیا این سلول ها توسط اچ آی وی کشته شده اند و آیا خون را ترک کرده و به اندامهای لنفاوی می روند تا برای ایجاد یک واکنش ایمنی آماده شوند.
دو تا چهار هفته پس از مواجهه با ویروس، بالای ۷۰ درصد از افراد آلوده به اچ آی وی از علائمی شبیه سرماخوردگی که مربوط به عفونت حاد است رنج می برند. سیستم ایمنی بدن بیمار با سلول های کشنده T سلولهای (CD8 + T) و سلول تولید پادتن های B در حال مبارزه بوده، که به طور چشمگیری سطح اچ آی وی را کاهش می دهد. تعداد سلول های CD4 + T در بیماران ممکن است به ۸۰ تا ۹۰ درصد از سطح اولیه خود برگردد. بعد از آن ممکن است فرد از علائم مرتبط با اچ آی وی برای سالها با وجود تکرار مداوم کشت اچ آی وی در اندامهای لنفاوی در مرحله فاز حاد عفونت باقی بماند.
یکی از دلایلی که HIV منحصر به فرد است این است که با وجود واکنش های ایمنی تهاجمی بدن، که برای پاکسازی عفونت های ویروسی کافی می باشند، برخی ویروس های HIV بطور ثابت می گریزند. این امر در شرف ورود به بخش بزرگتر و در میزان بالایی از جهش هایی است که در طول فرآیند تکثیر اچ آی وی رخ می دهند. حتی زمانی که این ویروس با جهش از سیستم ایمنی بدن دوری نمی کند بهترین سربازان بدن در مبارزه با اچ آی وی و زیر مجموعه های خاصی از سلول های کشنده Tمی باشند، ممکن است آنچنان به سرعت تکثیر یابند که عفونت اولیه به دنبال آن ایجاد شده که می تواند این سربازان را خسته و ناپدید کند، و اجازه دهد اچ آی وی گریخته و به تولید و نسخه برداری ادامه دهد.
علاوه بر این، در اوایل دوره عفونت اچ آی وی، بیماران ممکن است واکنش سلولهای CD4 + T که مخصوص اچ آی وی هستند آن را شکست داده و به طور معمول سرعت تکثیر ویروس را کند سازد. چنین واکنش هایی شامل ترشح اینترفرون و دیگر عوامل ضد ویروسی، و ارکستراسیون سلول های CD8 + Tمی باشد.
روند عفونت اچ آی وی
در میان بیماران ثبت نام شده در مطالعات بزرگ واگیرشناسی در کشورهای غربی ، زمان متوسط از عفونت با HIV تا رشد و افزایش علائم مربوط به ایدز ، در حدود ۱۰ تا ۱۲ سال است. با این حال محققان تنوع گسترده ای در پیشرفت بیماری مشاهده کرده اند. علائم حدود ۱۰ درصد از افراد آلوده به HIV در این مطالعات در طی دو تا سه سال اول پس از عفونت به ایدزپیشرفت کرده است، در حالی که در بیش از۵ درصد از افراد مورد مطالعه، تعداد سلولهای CD4 + T ثابت بوده و حتی پس از ۱۲ سال یا بیشتر هیچ علائمی دیده نشده است .
عواملی مانند سن و یا تفاوت های ژنتیکی بین افراد، سطح عفونت زایی اختصاصی ویروس ها و عفونت همزمان با سایر میکروبها ممکن است بر میزان و شدت پیشرفت بیماری تاثیر بگذارد. داروهایی که با عفونت مرتبط با ایدز در ارتباط هستند با جلوگیری و یا درمان بیماری هایی از قبیل ذات الریه پنومونی کارینی، طول زندگی افراد آلوده به اچ آی وی را افزایش داده و بهبود بخشیده اند.
هم گیرنده های اچ آی وی و پیشرفت بیماری
تحقیقات اخیر نشان داده است که بسیاری از گونه های آلوده کننده اچ آی وی علاوه بر مولکول CD4، از یک مولکول هم گیرنده به نام CCR5 استفاده می کند، تا به برخی از سلول های مورد هدف خود وارد شود. افراد آلوده به اچ آی وی با یک جهش خاص در یکی از دو نسخه ژن برای این گیرنده، به طور کلی یک دوره بیماری کندتر را نسبت به افراد با دو نسخه ژن عادی ایجاد می کند. افراد بسیار کمی هستند که با دو نسخه جهش یافته ژن CCR5 دیده می شوند –که در اکثر موارد – به طور کامل از عفونت HIV محافظت می شوند. جهش در ژن اچ آی وی در دیگر هم گیرنده ها نیز ممکن است بر میزان پیشرفت بیماری تاثیر بگذارد.
میزان و مقدار ویروس پیشرفت بیماری را پیش بینی می کند
مطالعات متعدد نشان می دهد که در افرادی با سطوح بالایی از اچ آی وی در خون ، احتمال ابتلا به علایم جدید مرتبط با ایدز بیشتر بوده و یا مرگ و میر آنها نسبت به افراد با سطح پایین تری از ویروس بیشتر می باشد. به عنوان مثال، در مطالعه کوهورت چند مرکز ایدز (MACS)، محققان حمایت کننده NIAID اثبات کردند که سطح اچ آی وی در پلاسما فرد به زودی پس از عفونت که”آخرین میزان” ویروسی هم نامیده می شود با توجه به میزان پیشرفت بیماری کاملا قابل پیش بینی است ؛ به این معنی که، در بیماران با سطح بالایی از ویروس احتمال بیشتری برای بیشتر و سریع تر مریض شدن، نسبت به افراد با سطوح پایین ویروس وجود دارد. MACS و مطالعات دیگر دلایل اصلی برای درمان ضد ویروس پسگرد تهاجمی برای افراد آلوده به اچ آی وی را فراهم کردند، و همچنین به طور معمول از آزمایش خون های جدید و در دسترس برای اندازه گیری میزان ویروس هنگام شروع، نظارت و اصلاح درمان ضد اچ آی وی استفاده کرده اند.
ترکیبات دارویی جدید ضد اچ آی وی – که به طور کلی شامل یک مهار کننده پروتئاز های گرفته شده با دو مهارکننده ترانس کریپتاز معکوس می باشند- می توانند “میزان ویروسی بودن” یک فرد را تا سطوح بسیار پایین کاهش دهند و در بسیاری از موارد پیشرفت بیماری اچ آی وی را برای دوره های طولانی به تاخیر بیاندازند. با این حال، رژیم های ضد پسگرد ویروسی هنوز به طور کامل و دائم ویروس را در افراد آلوده به اچ آی وی سرکوب می کنند. مطالعات اخیر نشان داده است که اچ آی وی به نسخه برداری و تکثیر -به شکل ماهرانه ای در سلولهای CD4 + T باقیمانده ادامه می دهد حتی در بیماران تحت درمان با داروهای ضد ویروس تهاجمی که اچ آی وی به راحتی در خون آنها قابل تشخیص نیست. محققان در سراسر جهان در حال کار برای تولید نسل بعدی از داروهای ضد اچ آی وی هستند.
اچ آی وی فعال در غدد لنفاوی
اگر چه در افراد آلوده به اچ آی وی غالبا یک دوره طولانی از زمان تاخیر بالینی وجود دارد و نشانه های کمی از این بیماری دیده می شود،اما ویروس هرگز واقعا نهفته نمی باشد. محققان NIAID نشان داده اند که حتی در اوایل بیماری، HIV به طور فعال در غدد لنفاوی و اندام های مربوطه تکثیر می شود که در آنجا مقدار زیادی از ویروس در شبکه های سلول های خاص بوسیله یک شاخک اضافی بلند و حساس به دام می افتند. این سلول ها سلولهای دندریتیک فولیکولار (FDCs) نامیده می شود.
FDCs در نواحی ناآرام فعالیت های ایمنی به نام مراکز نمو و زایش واقع شده اند. آنها مانند کاغذ سمی مگس کش عمل می کنند، پاتوژن های مهاجم (از جمله HIV) را به دام انداخته و آنها را تا زمانی که سلول های B برای شروع یک واکنش ایمنی برسند، نگاه می دارند.
درست پشت سر سلول های B، سلولهای CD4 + T قرار دارند که به مراکز نمو و زایش حمله برده تا به سلول های B که در حال مبارزه با اشغالگران هستند کمک کنند. سلولهای CD4 + T، که هدف اصلی اچ آی وی می باشند، ممکن است هنگام روبرو شدن با ویروس اچ آی وی که به دام FDCs افتاده اند، آلوده شوند. تحقیقات نشان می دهد که HIV به دام افتاده در FDCs عفونی باقی می ماند، حتی زمانی که با پادتن پوشیده شوند. بنابراین، FDCs یک مخزن مهم اچ آی وی بوده و مقدار زیادی از عفونت اچ آی وی به دام افتاده در FDCs ممکن است برای جایی که حرکت عفونت اچ آی وی ثابت می ماند توجیه شود.
پس از آلوده شدن، سلولهای CD4 + T ممکن است مرکز نمو و زایش را ترک کرده و سلول های دیگر CD4 + که در مناطقی از گره های لنفاوی اطراف مرکز نمو جمع شده اند را آلوده کند.
در بیش از یک دوره از سال ها، حتی زمانی که ویروس کمی در خون قابل تشخیص است، مقدار قابل توجهی از ویروس در مراکز نمو جمع می شوند، و هم درون سلول های آلوده و هم FDCs را آلوده می سازند. در داخل و اطراف مراکز نمو، سلولهای CD4 + T متعدد احتمالا با افزایش تولید سایتوکاین مانند TNF-alpha و IL-6 فعال می شوند، که احتمالا توسط سلول های B ترشح می شوند. فعال سازی سلول های سالم اجازه می دهد تا به راحتی آلوده تر شده و تکثیر اچ آی وی در سلولهایی که در حال حاضر آلوده می باشند، افزایش یابد.
در حالی که مقادیر بیشتر از سایتوکاین های خاص مانند TNF-alpha و IL-6 در طول عفونت اچ آی وی ترشح می شوند، بقیه که دارای نقش های کلیدی در تنظیم عملکرد سیستم ایمنی طبیعی هستند ممکن است در مقادیر کم ترشح شوند. به عنوان مثال، سلولهای CD4 + T ممکن است توانایی خود را برای تولید اینترلوکین ۲ (IL-2) و سایتوکاین که باعث افزایش رشد دیگرسلول های T می شود و به تحریک واکنش سلول های دیگر به مهاجمان کمک می کند، از دست بدهند. سلول های آلوده نیز سطوح پایینی از گیرنده های IL-2 را دارا بوده، که ممکن است توانایی آنها برای واکنش به سیگنال از سلول های دیگر کاهش یابد.
شکسته شدن شبکه های FDC
در نهایت، اچ آی وی انباشته شده شبکه FDC را تحت تاثیر قرار می دهد همانطور که این شبکه می شکند، ظرفیت به دام انداختن آنها نیز مختل شده و مقدار زیادی از ویروس وارد جریان خون می شود.
اگر چه هنوز مشخص نیست که چرا FDCs از بین می رود و شبکه های FDC متلاشی می شوند، اما برخی از دانشمندان فکر می کنند که این روند ممکن است در بیماریزایی اچ آی وی به اندازه از دست دادن سلولهای CD4 + T مهم باشد. تخریب ساختار گره های لنفاوی که در اواخر بیماری اچ آی وی مشاهده می شود ممکن است مانع یک واکنش ایمنی موفق در برابر نه تنها اچ آی وی بلکه دیگر عوامل بیماری زا باشد. این نابودی نشانه شروع عفونت های فرصت طلب و سرطانها که مشخصه ایدز هستند، می باشد.
نقش سلول های CD8 + T
نقش سلولهای CD8 + T در واکنش ایمنی به اچ آی وی در طول عفونت حاد و مرحله نهفته بیماری بالینی مهم است. این سلول ها به سلول های آلوده که در حال تولید ویروس هستند حمله کرده و آنها را نابود می کنند.
همچنین سلولهای CD8 + T به نظر می رسد با ترشح محلولی تکثیر اچ آی وی را سرکوب می کنند. به نظر می رسد چند مولکول، از جملهRANTES، MIP-1alpha، MIP-1beta، و MDC تکثیر اچ آی وی را با اشغال هم گیرنده های لازم برای ورود به برخی از گونه های اچ آی وی درون سلول های مورد هدف، مسدود می سازند. ممکن است بسیاری از دیگر مولکول های سیستم ایمنی بدن که هنوز کشف نشده اند تکثیر اچ آی وی را تا حدودی انجام دهند.
تکثیر سریع و جهش اچ آی وی
اچ آی وی به سرعت تکثیر می شود؛ چند میلیارد ذره ویروس جدید ممکن است هر روز تولید شوند. علاوه بر این، آنزیم ترانس کریپتاز معکوس اچ آی وی هنگام تولید نسخه DNA از HIV RNA دچار اشتباه می شود. در نتیجه، بسیاری از انواع HIV در یک فرد بوجود می آید، که برخی از آنها ممکن است توسط پادتن و یا سلولهای کشنده T از بین بروند. علاوه بر این، اچ آی وی می تواند با خود ترکیب شده و طیف گسترده ای از انواع اچ آی وی را تولید کند.
در طول دوره بیماری اچ آی وی، گونه های ویروسی که در یک فرد آلوده پدیدار می شوند به طور گسترده ای در توانایی شان برای آلوده کردن و کشتن انواع سلول های مختلف، و همچنین در میزان تکثیر متفاوت هستند. دانشمندان در حال بررسی هستند که چرا گونه های اچ آی وی از بیماران مبتلا به بیماری پیشرفته به نظر خطرناک تر و آلوده تر از انواع سلول های گونه پیشین و مراحل اولیه بیماری در همان شخص می باشند.
نظریه هایی درباره اینکه سیستم ایمنی بدن در عفونت اچ آی وی سلول از دست می دهد
محققان در سراسر جهان در حال مطالعه هستند که چگونه اچ آی وی سلولهای CD4 + را از بین برده یا غیر فعال می کند ، و بسیاری فکر می کنند که تعدادی از مکانیسم ها ممکن است به طور همزمان در یک فرد آلوده به اچ آی وی رخ دهد. داده های اخیر نشان می دهد که میلیاردها سلول CD4 + T ممکن است هر روز از بین رفته، در نهایت توانایی احیا کننده سیستم ایمنی بدن را از توان بیاندازد.
کشته شدن سلول ها بطور مستقیم
زمانی که مقادیر زیادی از ویروس تولید شده و از سطح سلول جوانه زده، غشاء سلول را پاره کرده، یا زمانی که پروتئین های ویروسی و اسیدهای نوکلئیک در داخل سلول جمع شده، و اندامگان سلولی را دچار اختلال می کنند، سلولهای CD4 + T آلوده ممکن است به طور مستقیم از بین بروند.
تشکیل پیوسته یاخته
سلول های آلوده نیز ممکن است با سلول های سالم نزدیک خود ترکیب شده، و سلول های بزرگی شبیه بالون به نام پیوسته یاخته را بوجود آورند در آزمایشات در NIAID و جاهای دیگر، این سلول های غول پیکر با مرگ سلولهای سالم در ارتباط می باشند. حضور گونه هایی از اچ آی وی که پیوسته یاخته نیز نامیده می شوند با پیشرفت سریع بیماری در افراد آلوده به اچ آی وی در ارتباط است.
آپوپتوز (مرگ سلولی برنامه ریزی شده)
سلولهای CD4 + T آلوده ممکن است زمانی کشته شدند که قوانین سلولی توسط پروتئین اچ آی وی تحریف شده، و احتمالا منجر به خودکشی آنها شده که به عنوان مرگ سلولی برنامه ریزی شده یا آپوپتوز شناخته شده است. گزارش های اخیر نشان می دهد که آپوپتوز به میزان بیشتری در افراد آلوده به اچ آی وی، هم در جریان خون و هم غدد لنفاوی روی می دهد.
سلول های سالم نیز ممکن است آپوپتوز را انجام دهند. محققان در کشت سلولی نشان دادند که پوششاچ آی وی به تنهایی و یا پیوست شده به پادتن ها یک سیگنال نامناسب به سلولهای CD4 + T می فرستند باعث را مرگ آنها می شود حتی اگر به ویروس اچ آی وی آلوده نباشند.
تماشاگران بی گناه
سلول های سالم ممکن است در یک سناریوی تماشاچی بی گناه از بین بروند: ذرات اچ آی وی ممکن است به سطح سلول متصل شده، به آنها ظاهر یک سلول آلوده را داده و آنها را برای تخریب توسط سلولهای T کشنده نشاندار کند.
سلول های کشنده T نیز ممکن است به اشتباه سلولهای سالمی را نابود کند که ذرات اچ آی وی را نابود کرده اند و تکه هایی از اچ آی وی بر روی سطح آنها نمایان می شود. متناوبا، از انجا که پوشش پروتئینی اچ آی وی دارای شباهت هایی به مولکول های خاص در سلولهای CD4 + Tاست، واکنش ایمنی بدن ممکن است به اشتباه به این سلول ها نیز آسیب بزند.
آنرژی (بی رمقی)
محققان در کشت سلولی نشان داده اند که سلول های CD4 + T را می توان با یک سیگنال از اچ آی وی غیرفعال کرد که آنها را نسبت به واکنش به تحریک های سیستم ایمنی به حالت ناتوان رها کرد. این حالت غیر فعال به عنوان آنرژی شناخته شده است.
سوپرپادزا
دیگر محققان پیشنهاد کرده اند که یک مولکول شناخته شده به عنوان یک سوپرپادزا،یا توسط اچ آی وی یا یک عامل نامربوط ایجاد می شود، ممکن است در مقادیر انبوه سلولهای CD4 + T را به یک باره تحریک کند، آنها را بسیار مستعد برای ابتلا به عفونت اچ آی وی عرضه کرده و متعاقبا باعث مرگ سلول ها شود.
آسیب به سلول های پیشرو
مطالعات نشان می دهد که اچ آی وی همچنین سلول های پیشرو که بالغ شده اند و وظیفه خاصی درسیستم ایمنی بدن دارند، و همچنین بخش هایی از مغز استخوان و غده تیموس که برای رشد چنین سلولهایی مورد نیاز هستند را از بین می برد. این اندام ها احتمالا توانایی ترمیم خود را از دست می دهند، و با سرکوبی بیشتر سیستم ایمنی بدن از بین می روند .
آسیب به سیستم عصبی مرکزی
اگر چه مونوسیت ها و ماکروفاژها می توانند با اچ آی وی آلوده شوند، اما به نظر می رسد آنها به نابودی نسبتا مقاوم هستند. با این حال، این سلولها در سراسر بدن حرکت کرده و ویروس اچ آی وی را به اندام های های مختلف، به خصوص ریه ها و مغز می برند. افراد آلوده به اچ آی وی اغلب اختلال در سیستم عصبی مرکزی را تجربه کرده اند. بروز بیماری های عصبی اچ آی وی، در ۴۰ تا ۵۰ درصد از افراد آلوده به اچ آی وی دیده می شود، که موضوع بسیاری از پروژه های تحقیقاتی است. محققان حدس میزنند که تجمع اچ آی وی در مغز و سلول های عصبی و یا انتشار نامتناسب سیتوکین یا محصولات فرعی سمی توسط این سلول ها، ممکن است دلیل آن باشد.
نقش فعال سازی ایمنی در بیماریاچ آی وی
در طول یک پاسخ ایمنی طبیعی، بسیاری از اجزای سیستم ایمنی بدن برای مبارزه با مهاجم بسیج می شوند. به عنوان مثال، سلولهایCD4 + T ممکن است به سرعت تکثیر شده و ترشح سیتوکین را افزایش دهند، در نتیجه، سیگنال می فرستد که سلول های دیگر وظایف خاص خود را انجام دهند. سلول های زباله خوار به نام ماکروفاژ ممکن است دو برابر شده و اندامکها متعددی رشد می کنند ، از جمله لیزوزومها که حاوی آنزیم های گوارشی هستند و برای فرایند هضم پاتوژن ها بکار می روند. هنگامی که سیستم ایمنی آنتی ژن های خارجی را از بین برده و پاکسازی کرد، به حالت آرامش نسبی برمی گردد.
برعکس، با وجود آن که اچ آی وی در نهایت باعث ضعف سیستم ایمنی بدن می شود، این بیماری به علت بیشتر عملکردهایش توسط پرکاری سیستم ایمنی بدن مشخص می شود که عواقب منفی دارد. همانطور که در بالا اشاره شد، تکثیر اچ آی وی و گسترش آن بر روی سلول های فعال شده CD4 + تاثیر زیادی دارد. فعال شدن مزمن سیستم ایمنی بدن در طول بیماری اچ آی وی نیز ممکن است به تحریک عظیم سلول های B یک فرد منجر شده ، آسیب رسیدن به توانایی این سلول ها ، پادتن ها را بر علیه دیگر عوامل بیماری زا ایجاد می کند.
فعالسازی مزمن ایمنی بدن همچنین می تواند منجر به آپوپتوز، و افزایش تولید سیتوکین شود که ممکن است نه تنها تکثیر اچ آی وی را افزایش دهد بلکه منجر به اثرات مخرب نیز شود. برای مثال، افزایش سطح TNF-آلفا، ممکن است حداقل تا حدی برای از دست رفتن شدید وزن یا سندرم اتلاف در بسیاری از افراد آلوده به اچ آی وی مسئول باشد.
تداوم اچ آی وی و تکثیر اچ آی وی احتمالا نقش مهمی در حالت فعالسازی مزمن دستگاه ایمنی بدن داشته که در افراد آلوده به اچ آی وی دیده می شود. علاوه بر این، محققان نشان داده اند که عفونت دیگر اندامگان سلول های سیستم ایمنی را فعال کرده و تولید این ویروس را در افراد آلوده به اچ آی وی افزایش می دهد.فعالسازی ایمنی بدن به عفونت مقاوم ، و یا برگشت مجدد و عود فعالسازی سیستم ایمنی و انفجار تولید ویروس منجر شده، و به احتمال زیاد به پیشرفت بیماری اچ آی وی کمک می کند.
پژوهش NIAID بر روی پاتوژنز ایدز
دانشمندان حامی NIAID که تحقیقات پاتوژنز اچ آی وی را در آزمایشگاهی در محوطه موسسه ملی بهداشت (NIH) در بتسدا ، در آزمایشگاه راکی مانتین مؤسسه در همیلتون، و در دانشگاه ها و مراکز پزشکی در ایالات متحده و خارج از کشور انجام داده اند .
یک مرکز مشترک مورد حمایت NIAID از سازمان بهداشت جهانی، تحقیقات ایدز NIH و برنامه معرفی مرجع، مواد تحقیقاتی رایگان مرتبط با ایدز پژوهشگران واجد شرایط را در سراسر جهان فراهم می کند.
علاوه بر این، موسسه گروهی از محققان و کمیته های مشورتی را برای تبادل اطلاعات علمی، روشن سازی اولویت های پژوهشی و تحقیقاتی فرا خوانده و نیازها و فرصت ها را برای توجه جامعه علمی ارائه می کند.
واژه نامه
آپوپتوز – خودکشی سلولی، همچنین به عنوان مرگ سلولی برنامه ریزی شده شناخته شده است. اچ آی وی ممکن است آپوپتوز را در هم سلول های سیستم ایمنی آلوده و هم سالم القا کند.
سلول های B: سلول های سفید خون درسیستم ایمنی بدن که برای تولید پروتئین های مقابله کننده با عفونت به نام پادتن می باشند.
سلولهای CD4 + T -: سلول های سفید خون که هماهنگ کننده واکنش های ایمنی بوده، به سلول های دیگر در سیستم ایمنی بدن برای انجام وظایف خاص خود پیام می فرستد. همچنین به عنوان سلول های کمک کنندهT شناخته شده اند، این سلول ها در طول عفونت HIV غیر فعال شده و از بین می روند.
سلول های CD8 + T -: سلول های سفید خون که سلول های آلوده به HIV و یا ویروس های دیگر ، و یا سلول های تبدیل شده به سرطان را از بین می برند. این سلول ها همچنین محلولی را تراوش می کنند که ممکن است HIV را بدون کشتن سلول های آلوده به طور مستقیم سرکوب می کند.
سیتوکین : پروتئین که برای ارتباطات توسط سلول های سیستم ایمنی بدن استفاده می شود که نقش اصلی را در مقررات عادی واکنش ایمنی دارد.
سیتوپلاسم : ماده زنده در درون یک سلول.
سلولهای دندریتیک : سلول های سیستم ایمنی با شاخکی بلند و حساس. برخی از این سلول های خاص در مخاط بوده که ممکن است بعد از رابطه جنسی به HIV متصل شده و ویروس را از محل عفونت به غدد لنفاوی حمل کنند. به سلولهای دندریتیک فولیکولی مراجعه کنید.
آنزیم : یک پروتئین که واکنش شیمیایی را تسریع کرده در حالیکه خود بدون تغییر باقی می ماند.
سلول های فولیکولی دندریتیک (FDCs) – سلول های موجود در مراکز نمو و زایش (مناطق سلول B) در اندامهای لنفاوی. FDCs دارای شاخکهای نخ مانندی هستند که یک شبکه تور مانند را برای به دام انداختن متجاوزان تشکیل داده و آنها را به سلولهای B تحویل می دهد، که پس از آن پادتن ها را مجبور می سازد که به مهاجمان حمله کنند.
مراکز نمو و زایش – ساختارها در بافتهای لنفاوی که حاوی FDCs و سلول های B بوده، و واکنش های ایمنی در آنها آغاز می شود.
gp41: گلیکوپروتئین ۴۱، یک پروتئین جاسازی شده در پوشش بیرونی HIV می باشد. نقش کلیدی را در HIV برای ابتلا سلول هایCD4 + T دارد که ترکیب غشاء های ویروسی و سلول را تسهیل می سازد.
gp120: گلیکوپروتئین ۱۲۰، یک پروتئین که از سطح اچ آی وی بیرون زده و به سلولهای CD4 + T متصل می شود.
gp160: گلیکوپروتئین ۱۶۰، یک پروتئین پیشرو اچ آی وی است که توسط آنزیم پروتئاز HIV به gp41 gp120 تقسیم می شود.
اینتگراز – یک آنزیم HIV که توسط ویروس برای ادغام مواد ژنتیکی درون DNA سلول میزبان بکار می رود.
سارکوم کاپوزی – یک نوع از سرطان است که با رشد غیر طبیعی عروق خونی مشخص می شود که ضایعات بنفش و یا قهوه ای را ایجاد می کند.
سلول های کشنده T : به سلولهای CD8 + T مراجعه کنید.
لنتی ویروس – ویروس “آهسته” که مدت زمان طولانی بین عفونت و شروع علائم وجود دارد. اچ آی وی همانند ویروس نقص ایمنی میمون (SIV)، که پستانداران غیرانسان را آلوده می کند یک ویروس آهسته است.
LTR : تکرار ترمینال طولانی ، توالی RNA که در هر دو انتهای ماده ژنتیکی اچ آی وی تکرار می شوند. این سوئیچ ها نظارتی ممکن است به کنترل نسخه برداری ویروسی کمک کند.
اندامهای لنفاوی : شامل لوزه ها، لوزه سوم، غدد لنفاوی، طحال و بافت های دیگر می باشند. به عنوان سیستم فیلترکننده بدن عمل می کنند، مهاجمان را به دام انداخته و آنها را به گردان سلول های ایمنی تحویل داده که در آنجا جمع می شوند.
ماکروفاژ : یک سلول بزرگ سیستم ایمنی بدن است که عوامل پاتوژن و سایر مزاحمان را می بلعد. دیگر سلول های سیستم ایمنی را با تکه های کوچکی از مهاجمان تحریک می کند.
مونوسیت: سلول های سفید خون است که به صورت یک ماکروفاژ رشد می کنند وقتی که وارد بافت می شوند.
عفونت های فرصت طلب: بیماری ناشی از یک ارگانیسم است که معمولا در یک فرد با یک سیستم ایمنی طبیعی باعث بیماری می شود. افراد مبتلا به عفونت پیشرفته اچ آی وی از عفونت فرصت طلبا ریه ها، مغز، چشم و اندام های دیگر رنج می برند.
پاتوژنز: تولید و یا رشد یک بیماری است. ممکن است تحت تاثیرعوامل بسیاری، از جمله میکروب های آلوده کننده و واکنش ایمنی میزبان باشد.
پروتئاز: یک آنزیم اچ آی وی است که برای برش پروتئین اچ آی وی بزرگ به تکه های کوچکتر مورد نیاز برای مونتاژ یک ذره ویروس عفونی بکار می رود.
ویروس اولیه: DNA یک ویروس، مانند اچ آی وی است که در ژن های سلول میزبان ادغام می شود.
ویروس پسگرد: اچ آی وی و دیگر ویروس هایی که مواد ژنتیکی را به شکل RNA حمل کرده و دارای آنزیم ترانس کریپتاز معکوس می باشند.
ترانس کریپتاز معکوس: آنزیم تولید شده توسط اچ آی وی و دیگر ویروس های پسگرد که اجازه می دهد تا آنها DNA را از RNA سنتز کنند.
پیوسته یاخته: سلول های بزرگ که بوسیله ترکیبی از سلول های دیگر تشکیل می شوند.
NIAID: بخشی از موسسه ملی بهداشت، که از پژوهش ها درباره ایدز، سل و سایر بیماری های عفونی و همچنین آلرژی و ایمن شناسی حمایت می کند.
ترجمه شده از وبسایت: www.webmd.com
مطالب ویژه نسخه

مصرف بیش از حد این ۸ ماده غذایی بینهایت خطرناک است

شیرین کننده مصنوعی چیست، فواید و مضرات آن کدام است؟

۱۴ دلیلی که نشان میدهد چرا شما همیشه گرسنه هستید
قبل از اهدای خون چه چیزی بخوریم و چه چیزی نخوریم

چند نکته مهم در تعیین اهداف و رشد شخصی (بخش اول)
آخرین مطالب

لیست بهترین متخصص ارتودنسی در چیذر و نواحی اطراف آن
لیست متخصص ارتودنسی در دروس و اطراف آن